2022年5月12日,同济大学生命科学与技术学院王红兵教授课题组在《FrontiersinAgingNeuroscience》杂志在线发表题为“Autophagy regulation influences β-amyloid toxicity in transgenic Caenorhabditis elegans”的研究论文,该研究以淀粉样蛋白(Aβ)转基因秀丽隐杆线虫为模型揭示了Aβ毒性与自噬异常之间的分子机制。
阿尔兹海默症(AD)是一种常见的神经退行性疾病,Aβ蛋白的异常积累被认为是AD的一个重要病因。然而目前针对Aβ蛋白的抗体药物如:Aduhelm在AD的晚期治疗中疗效较为有限。其原因主要是AD病情发展产生的一系列并发症加剧了神经元的损伤,破坏了脑内蛋白稳态。研究者们发现在AD患者的脑切片及转基因Aβ小鼠脑切片中存在严重的自噬体积累现象。这标志着自噬受损可能是Aβ毒性破坏稳态后的下游事件。然而自噬体积累与Aβ毒性之间的联系仍不明确,自噬调节在AD发生发展过程中的作用尚不清晰。
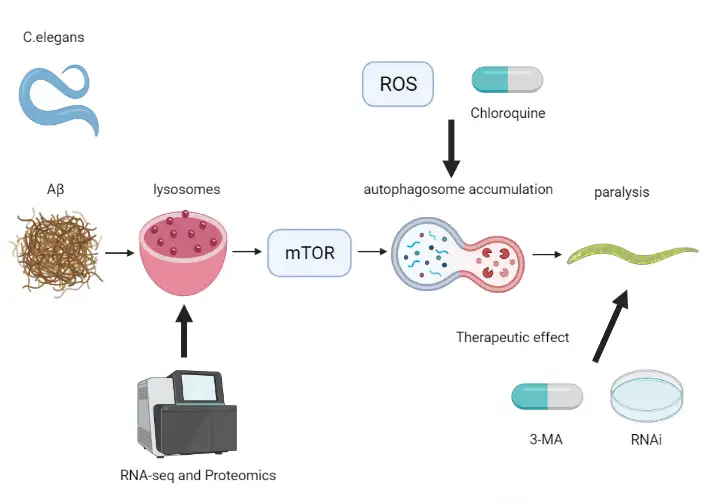
在本项研究中,课题组利用转录组学测序(RNA-seq)和非标定量质谱蛋白组学,确认了转基因Aβ线虫中自噬及自噬相关信号通路的异常。通过显微注射实现了转基因Aβ线虫自噬体的GFP-mCherry红绿双荧光标记。利用该模型和现代分子生物学技术,发现自噬体积累并不与衰老导致的溶酶体活性降低有关,而是由自噬体与溶酶体异常融合所导致。结合小分子探针技术进一步研究发现,抑制自噬体形成,从而减少自噬体积累能够缓解Aβ线虫体内的氧化应激水平。相反破坏溶酶体中的酸性环境,将显著加剧Aβ的毒性效应,加速Aβ线虫的瘫痪。此外还发现了在自噬异常的情况下,小分子伴侣蛋白HSP-70、HSP-16.2在维持蛋白稳态中发挥重要作用,存在潜在代偿机制。这说明改善自噬异常在AD的治疗中非常重要,本研究为寻找AD治疗靶点、探明发病机制提供了新的理论依据。
博士生林鸿儒为本文第一作者,博士生高叶慧、张辰,硕士生马博天、吴萌晨参与了该研究,王红兵教授、崔香环老师为本文共同通讯作者。本研究得到国家自然科学基金、上海市科委及同济大学等项目资助。