耐药性细菌横行,寻找新的抗菌剂已经迫在眉睫
致病性细菌在全球范围内威胁着人类的健康,由致病菌引起的伤口感染给患者带来了巨大痛苦和经济损失。使用抗生素杀菌是治疗伤口感染的经典疗法,然而抗生素的误用和滥用导致了部分细菌产生了耐药性。此外,具有多重耐药性的“超级细菌”可能“免疫”大多数现有抗生素,并有可能进一步引起全球疫情。面对这一窘境,研究人员已使用多种材料以对抗细菌感染,如季铵离子、溶菌酶和金属离子等。但这些抗菌材料的应用受限于其固有的环境危害性、非广谱抗菌性和潜在的生物毒性。因此,开发对抗细菌感染的新型治疗策略势在必行。
四通道高效杀菌,“ROS飓风”内外夹击提供抗菌新思路
近期,来自四川大学的邓怡-杨为中团队与合作者等人开发了一种具备四通道杀菌能力的生物异质结平台,该材料搭载生长因子后可促进伤口皮肤组织修复。此研究工作从材料科学、细胞生物学、分子生物学和组织学水平对材料性能进行探究。该生物异质结平台具有光热、光动力、类POD和类GSHOx的特性,可引起外源性与内源性的“ROS飓风”,对细菌起到“内外夹击”的效果,达到高效杀菌的目的。进一步将FGF21接枝在生物异质结平台上,可加速受损皮肤自修复过程,为解决在复杂环境下进行感染性皮肤修复的难题提供了新的思路。相关工作以“Growth Factor-Decorated Ti3C2 MXene/MoS2 2D Bio-Heterojunctions with Quad-Channel Photonic Disinfection for Effective Regeneration of Bacteria-Invaded Cutaneous Tissue”为题发表于Small,来自四川大学的杨朝普和付馨靓(华西口腔甘雪琦老师研究生)为该论文的共同第一作者。
一、生物异质结平台的构建、抗菌机理及动物实验流程
如图1a所示,作者采用氢氟酸(HF)刻蚀MAX相陶瓷Ti3AlC2中的Al层后以制备MXene相材料Ti3C2,然后通过水热反应制备MXene/MoS2异质结材料。为提高材料的生物相容性,在材料表面建立了一层聚多巴胺涂层,最后接枝生长因子FGF21以增强材料促进皮肤自修复的能力,最终构建了一种具备四通道抗菌活性的生物异质结MXene/MoS2-FGF21 (MMF)。
根据生物异质结的类GSHOx和类POD性质探究结果与体外抗菌实验结果,该材料的抗菌机制被总结为光热、光动力、类POD和类GSHOx四通道协同抗菌。如图1b所示,材料在光照下引起外源性与内源性的“ROS飓风”,对细菌起到“内外夹击”的效果,达到高效杀菌的目的。
在动物实验中,作者选择了BALB/c小鼠建立感染伤口模型,将小鼠饲养至合适状态后利用其进行感染性皮肤伤口建模。待感染性伤口模型建立后,使用不同组别生物异质结材料对其进行光治疗,在后续时间段中观察其伤口恢复状况并记录小鼠体重等其他相关信息,一段时间后收集伤口组织和主要器官(心、肝、脾、肺以及肾)进行组织学分析。

图1. a) MXene、生物异质结、MoS2的制备示意图(虚线框内); b) 针对金黄色葡萄球菌的抗菌机制; c) 皮肤伤口感染模型的构建与治疗流程。
二、生物异质结体外抗菌效果
如图2a-d所示,使用不同材料光照处理并行涂布平板法后,各培养基上菌落数都有明显下降,异质结组均取得了较好的体外抗菌效果。为了直接观察细菌被破坏的情况,使用SEM观察了细菌的膜形态,如图2e、f所示,能够看出在取得了良好抗菌效果的组别中,细菌的膜结构被破坏,细菌主体坍缩,有内容物流出,证明了生物异质结在光照下能够破坏细菌的膜结构,进而杀灭细菌。针对细菌进行的活死染实验结果同样证明了异质结材料的优良抗菌效果(图2g、h,活细菌为绿色,死细菌为红色)。

图2. 抗菌性能实验:不同材料针对a)金黄色葡萄球菌和b)大肠杆菌涂布平板法结果;c)金黄色葡萄球菌和d)大肠杆菌菌落计数;e)金黄色葡萄球菌和f)大肠杆菌经过不同实验处理后的SEM图像(绿色箭头所指为细菌流出的内容物);g)金黄色葡萄球菌和h)大肠杆菌经过不同实验处理后的死活染图像。
三、生物异质结体内抗菌与促皮肤修复效果探究
为了验证所设计的生物异质结是否能够促进伤口愈合,作者设计了如图3a所示的动物实验,将小鼠饲养至合适状态后利用其进行感染性皮肤伤口建模,随后对其进行光治疗,在后续时间段中观察其伤口恢复状况并记录其他相关信息。如图3b所示,MMF组表现出了比其他组更快的伤口愈合速度,证明接枝了FGF21的生物异质结能够促进伤口愈合,进而降低伤口二次感染的风险。图3c是光治疗时小鼠伤口处的热成像图,图3f是具体的升温曲线。可以看出,PBS组虽然略有升温,但是尚未达到光热治疗所需温度,难以杀灭细菌。图3d展示的是取小鼠伤口处的组织液进行涂布平板法分析的结果,可以看出在进行光治疗后,伤口组织液中的细菌数量显著降低,可有效杀灭细菌,加快伤口皮肤愈合。这与利用伤口分泌物培养后计算得到的抗菌率吻合(图3g)。图3e是计算所得的伤口愈合率的统计数据,搭载了FGF21的组别有着更好的伤口恢复效果。
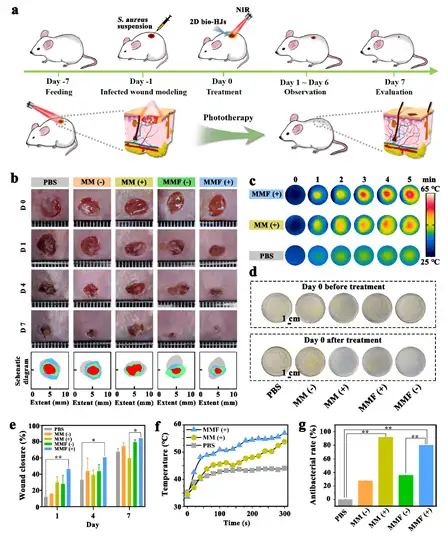
图3. 感染伤口愈合评估及动物抗菌试验:a)感染伤口模型的构建及伤口杀菌/愈合过程示意图;b)小鼠伤口伤口愈合过程的照片;c)光治疗时的实时红外热成像图;d)光治疗前后的伤口组织液的涂板结果
四、结论
该研究中开发的生长因子FGF21修饰的MXene/MoS2生物异质结表现出近红外光引起的光热和光动力效应。此外,材料可以释放出Mo4+离子,并在Mo4+与Mo6+的循环转化过程中,进行类POD反应和类GSHOx反应,不断积累细菌内源性ROS,消耗菌内GSH,从而使致病菌受到来自细菌内外的 “ROS飓风”攻击。在生物异质结上加载FGF21后,能有效促进细胞的迁移,增强伤口愈合能力,并展现出强大的杀菌效能。此外,该生物异质结还具有抗炎、增强胶原沉积、加速上皮和血管生成等作用,可加速皮肤创面愈合,在治疗感染性伤口过程中取得良好疗效。
文献链接
https://onlinelibrary.wiley.com/doi/10.1002/smll.202103993